採択課題
長期生存能を付与した肺癌に対するユニバーサルCAR-T細胞の開発
研究開発代表者
籠谷 勇紀
慶應義塾大学

悪性腫瘍に対するキメラ抗原受容体(chimeric antigen receptor: CAR)導入T細胞療法は難治がんを治癒に導き得る有望な治療法で、造血器腫瘍では実臨床での実績が蓄積している。その一方、患者から個別に細胞を製造する現行法ではコストが大きい上に、進行が早い症例では治療時機を逸するリスクや、患者ごとのT細胞の質の違いに伴う治療効果のばらつきなどの課題がある。
そこであらゆる患者に使用できるように健常人からCAR-T細胞を大量に製造する、「ユニバーサルCAR-T細胞」の開発が期待されており、コスト・治療効果双方で優れる可能性があるが、レシピエント・ドナー間のアロ免疫反応を制御する最適な方法が確立されていない。CRISPR/Cas9などのゲノム編集技術でCAR-T細胞のT細胞受容体(TCR)やHLAをノックアウトするアプローチが多くの場合とられているが、ゲノム編集に伴う安全上の懸念、細胞製造工程の複雑化、HLA欠損に伴うNK細胞からの攻撃回避の方法について懸念が残る。
上記の問題を解決するために、研究代表者は宿主からの免疫を逃れる手段としてウイルスが有する免疫制御関連タンパク質を利用することを着想し、タンパク質Aを発現させることでTCR発現を顕著に低下させ、アロ反応による細胞傷害活性を抑制できることを確認した。一方、NK細胞の活性化・抑制に関わる受容体発現プロファイルがドナーにより異なるというデータに基づき、HLAの抑制は行わず、アロ反応性を持つT細胞からの攻撃を回避する方法を計画した。
また、CAR-T細胞の治療効果は輸注細胞数だけでなく、未分化性を保持した長期生存能を有するT細胞の割合に強く依存する。研究代表者はPRDM1ノックアウトによりT細胞に長期生存能を付与できることをこれまでに示しており、この手法を進化させてCAR-T細胞の長期生存能とエフェクター機能を同時に高められる方法を確立する。
以上のように、本研究ではゲノム編集を用いないユニバーサルCAR-T細胞の開発を行い、臨床ステージアップに向けた準備を進める。標的疾患は、CAR-T細胞で一定の安全性が確立されている抗原が複数ある非小細胞肺癌とし、肺腺癌の90%以上の症例でMUC1、EGFRの共発現が見られることから、これらの抗原を標的として想定する。上記のアロ免疫回避機構、長期生存能を付与するエピゲノム改変を組込んだレンチウイルスベクターを開発し、in vivo腫瘍モデルで治療効果を確認する。
ユニバーサルCAR-T細胞のin vivoにおけるアロ反応の制御能については、臍帯血由来CD34陽性細胞をNOG-EXLマウスに生着させて作製するヒト化マウスを用いて評価する。ヒト造血の再構成後にCAR-T細胞を輸注し、免疫原性を評価する。さらに、腫瘍を移植するモデルで治療効果の評価も行う。不均一性の高い固形がんの性質を再現するため、肺癌臨床検体より樹立したオルガノイドを移植するゼノグラフトモデルを活用する。
これらの基礎研究開発を進めながら、知財戦略の策定、経営人材とのマッチング、具体的な事業計画の策定を進める。非臨床試験実施に向けて、治験で用いるレンチウイルス作製用プラスミド構築及び大量調製、PMDAとのRS戦略相談の対面助言完了までを目標とする。

図1:研究室メンバー
籠谷研究室|慶應義塾大学医学部・がん免疫研究部門|慶應義塾大学医学部・先端医科学研究所がん免疫研究部門(教授:籠谷勇紀)ではCAR-T細胞療法をはじめとする、がんに対する免疫療法の研究開発を行っております。
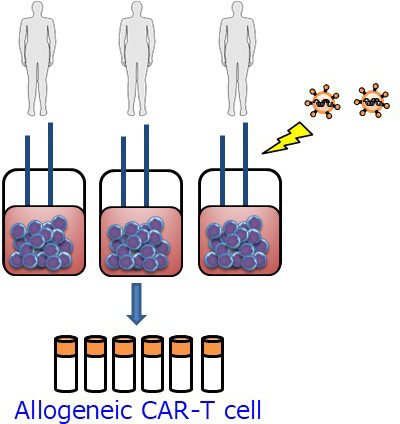
図2:本研究で開発するUniversal CAR-T細胞により、CAR-T細胞を安定的に大量製造できる。