採択課題
タンパク質補充療法の課題を克服するGain of Function酵素mRNA治療薬の開発
研究開発代表者
梅津 光央
東北大学

希少疾患のうち約80%は、特定のタンパク質の遺伝子が先天的に欠損・変異している遺伝性疾患です。遺伝性疾患を対象とした根本治療となる、欠損しているタンパク質を補充するタンパク質補充療法は、酵素タンパク質を補充する療法の市場だけでも世界市場は約86億ドル規模 (1兆2700億円, 2021年) に至り、今後さらに成長することが予測されます。補充するタンパク質は、欠損している同一のヒトタンパク質を補充することが基本ですが、近年、血友病B遺伝子治療では血小板増加症の原因遺伝子として同定された「野生型と比べて8倍高い血液凝固活性を有するFactor IX変異配列」が利用されています。この成果は、天然タンパク質よりも高い機能をもつアミノ酸配列へ改変 (Gain of Function: GOF) させた組換えタンパク質を用いることで、投与量を減少させ有効性や安全性を高める新規バイオ医薬品を開発できる可能性を示しています。
東北大学は、これまで自然界の進化を試験管内で模倣する進化分子工学に機械学習を組み入れることで、タンパク質の複数の機能・物性を同時に最適化設計できるaiProtein®技術を開発し、様々な抗体や酵素タンパク質の機能・物性を最適化してきました。タンパク質の特性(機能や物性)は、構成単位アミノ酸の配列だけで一義的に決まるが、アミノ酸配列の組み合わせ (配列空間)の規模は、実験的に作製し構造・機能を解析できるタンパク質の種類の数をはるかに上回ります。さらに、タンパク質の機能と物性(安定性・溶解性など)は反相関することが多いため、臨床試験へ展開できる程度まで機能と物性が同時に最適化したアミノ酸配列を取得できる確率は高くありません。東北大学・(株)レボルカは、aiProtein®技術により、目的の機能・物性が向上している変異体(アミノ酸配列の一部を改変させたタンパク質)を数%含んだ100個程度の変異体数のアミノ酸配列と特性(機能・物性)の実測値を紐づけた教師データによる機械学習から、複数の機能・物性を同時に向上・改変できる手法を開発しました。本事業では、このaiProtein®を使って高機能化(GOF化)酵素を創出し、mRNA治療と組み合わせることで、従来のタンパク質補充療法では実現できない「細胞内での治療効果の発揮」、「タンパク質医薬の複雑な製剤開発の回避」、「薬効継続性が長くかつ免疫刺激性を解決」を可能とするGOF化mRNA治療薬を開発し、遺伝性疾患の新たなモダリティを提案します。
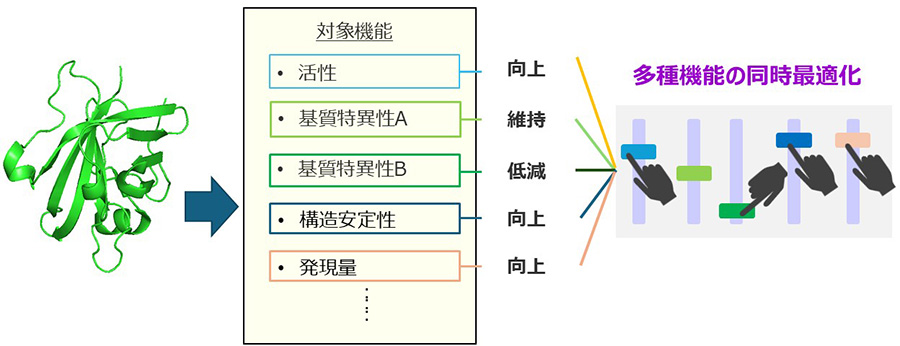
図1:aiProtein®:多種類の機能の同時最適化

図2:タンパク質補充療法とmRNA治療法の課題を克服した治療法の構築