採択課題
全身投与型マイクロRNA 抗腫瘍核酸医薬MIRX006の研究開発
研究開発代表者
高橋 陵宇
広島大学

本研究では、世界初のマイクロRNAシーズであるmiRNA-3140-3pと世界最先端の薬剤送達技術を組み合わせることで、全身投与型の新規抗がん核酸医薬として「MIRX006」の開発を行います(図1)。
miR-3140-3pは、広島大学・薬学部・細胞分子生物学研究室の基礎研究により同定されました。 無限に増殖するがん細胞に有限の寿命をもたらす「Aging switch」のコンセプトをもとに、これまでに約2000種類のマイクロRNAの中から細胞老化を誘導し、さらには、さまざまな種類のヒトのがん細胞株に対して増殖抑制効果を示すマイクロRNAを複数同定してきました(図2)。その中でもmiR-3140-3pが非常に強い抗腫瘍効果を示すことを明らかにしてきました。
現在、miR-3140-3pの局所投与製剤としてMIRX002を開発中であり、悪性胸膜中皮腫での非臨床有効性POCを取得しています(図3)。GLP毒性試験で安全性が確認されたのちに臨床試験に進んでいます。miR-3140-3pは強力なAPIであると考えられ、中皮腫に加え、頭頸部がん、食道がんなどの動物モデルにおいて抗腫瘍効果を示すことも確認できています。
MIRX002が局所投与型の薬剤であるのに対し、MIRX006は、非臨床・臨床で強力なAPIとして評価されてきたmiR-3140-3pの全身投与型の薬剤として開発が進められています。その送達技術には、静岡県立大薬学部の浅井知浩教授らにより開発されたpH応答性脂質であるDOP-TMDEDAから構成されるLNPを利用します。つまり、「MIRX006」は、腫瘍周辺のpHが酸性条件下ではカチオン性になるためがん細胞に選択的に取り込まれ有効性を示します。
本課題は、「生物学的評価及び臨床への繋ぎこみ」と「物性面の研究開発と製造開発」の2つの軸で構成され、さらに、スタートアップ (PURMX Therapeutics, Luna RD)と共同研究を行うことにより、「臨床ステージアップ」までの開発を目指します。
マイクロRNAは、siRNAと異なり、1つのマイクロRNAが複数の分子群を標的とします。このため、複数のシグナル経路に破綻が生じているがん細胞に対してマイクロRNAは有効に作用し、さらに、もともと生体内で作られる分子であることからも毒性が低いと考えられています。現時点で、マイクロRNA創薬の競合は世界的には複数社ありますが、マイクロRNAの標的特異性や薬剤送達技術を含む製剤開発の困難さから、非臨床の研究数はmRNAやsiRNAに比べ圧倒的に少なく、臨床開発に進んでいるものは極めて僅かです。また、がん治療薬として承認されたものはいまだありません。一方で、先行して開発を進めている局所投与型薬剤のMIRX002は、臨床試験に到達しており、現時点で重篤な副作用はいまだ観察されていません。
MIRX006製剤の生物学的評価は、マイクロRNAの評価を行ってきた広島大学が担当します。また、試験用製剤の製造からヒト臨床試験用のGMP製剤の開発といったCMC研究については静岡県立大学と広島大学GMPセンターが担当します。参加企業であるPURMX Therapeutics社は、現在、MIRX002の医師主導治験への製剤提供の他に、頭頚部がんに対する企業治験の実施や、複数適応に対するグローバル開発の準備を進めており、非臨床/薬事/製造/臨床の各分野に精通しています。また、FDAやPMDAなど規制当局との連携経験もあります。同社は、miR-3140-3pの知財を独占的に使用できることから、本研究においても製剤の CMC開発の支援、非臨床試験、臨床試験のプロトコル概要、TPPの設定、安全情報提供及びライセンス交渉の役割を担います。
「MIRX006」のプロトタイプ製剤を担がんマウスに尾静脈から全身投与した結果、正常組織では変化が観察されず、腫瘍に対して増殖抑制効果を示すことも確認できています。本研究が実現し、社会実装した場合、現在、希少疾患のみで成功している核酸医薬のがん領域への展開が一気に進むと期待されます。また、広島大学で構築された「マイクロRNAのスクリーニングプラットフォーム」と静岡県立大学で開発を継続している安全性に優れた「新規LNP技術」を組み合わせることにより、がん以外の疾患にも本邦独自の技術を応用でき、その成果は医薬品業界にパラダイムシフトをもたらすものと考えています。
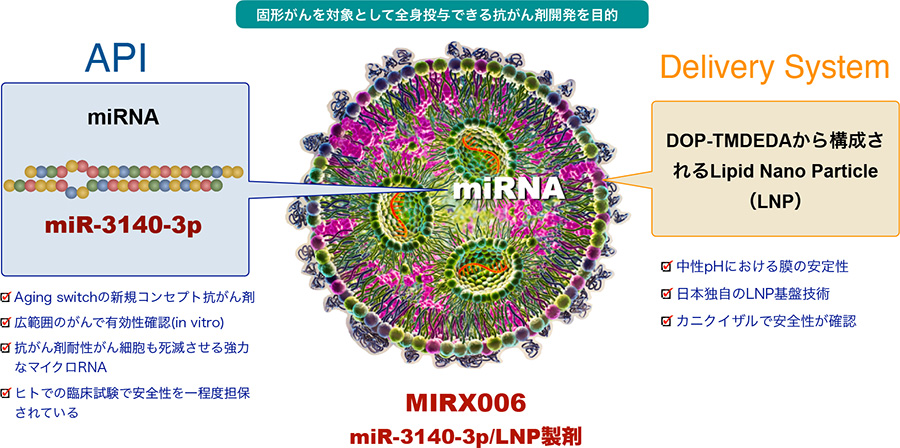
図1: miR-3140-3p/LNP製剤(MIRX006)の開発
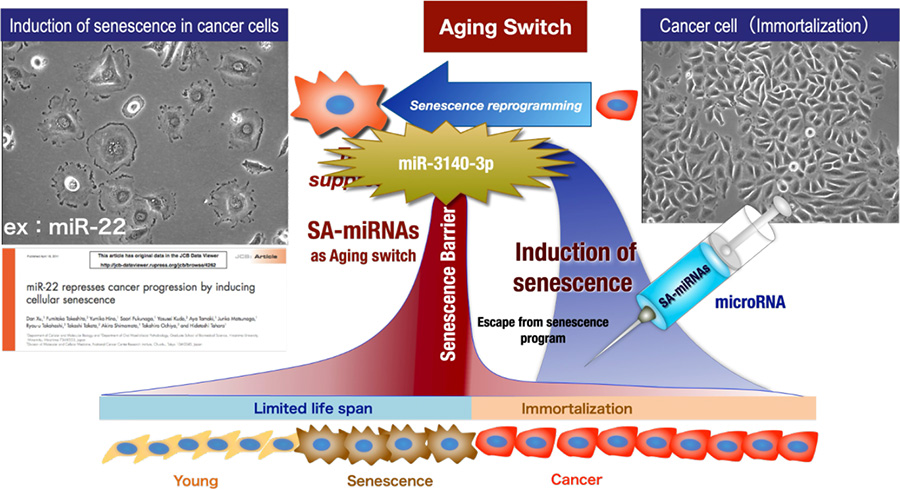
図2: Aging SwitchをコンセプトとしたマイクロRNA核酸医薬の開発

図3: MIRX002の抗腫瘍効果