採択課題
革新的核酸医薬技術を基盤とした神経・筋難病治療薬の開発
研究開発代表者
小比賀 聡
大阪大学

日本発の革新的バイオ医薬品の創出は喫緊の課題であり、様々な難病に対する核酸医薬の研究開発にも大きな期待が寄せられています。核酸医薬は従来の低分子医薬や抗体医薬では狙えない遺伝子を創薬ターゲットとする新しい創薬モダリティですが、副作用や標的臓器へのデリバリーシステムなどまだ課題も残されています。我々は、これまで長年にわたり核酸化学研究に取り組んでおり、その中で世界に先駆けて2’,4’-BNA/LNAと称する架橋型人工核酸の創製に成功してきました。また最近では、核酸医薬品の革新的基盤技術となる有効性向上のための人工核酸技術や安全性向上のための化学修飾、さらには脳や筋肉へ核酸医薬を送達させるデリバリー技術などを確立し、核酸医薬の抱える課題の幾つかを解決するとともに、一連の非臨床試験で人工核酸を搭載した核酸医薬の有効性や安全性を実証してきました(図1)。本研究課題では、大阪大学医学系研究科(木村康義特任講師)、京都大学医学研究科(尾野亘教授)、(株)レナサイエンス(平澤典保氏)、ルクサナバイオテク(株)(佐藤秀昭氏)とのオープンイノベーションに基づき、2つの核酸医薬シーズに対する研究開発を推進しています(図2)。
多系統萎縮症・パーキンソン病を対象としたシーズAでは、標的遺伝子のmRNAに対するギャップマー型アンチセンス核酸の配列最適化・構造最適化を現在進めています。多系統萎縮症(指定難病17)は国内で1.2万人が罹患する神経難病であり、現在のところ有効な治療薬はなく、対症療法も効果が極めて乏しいため、新たな治療法開発は喫緊の課題であるとされています。また、パーキンソン病(指定難病6)は国内の指定難病の中では罹患者が最も多く、2040年には世界で1000万人が罹患するとも言われています。これら神経変性疾患に対する治療薬の開発は、患者さんの予後改善、介護負担・社会負担の軽減に繋がることが期待されます。
一方、筋ジストロフィーを対象としたシーズBでは、創薬標的となるmiRNAの機能を阻害するアンチmiRNA核酸の最適化を実施しています。遺伝性筋疾患である筋ジストロフィー(指定難病113)に対する現行の治療法の効果は限定的であり、新たな治療法の開発が切望されています。今回我々が開発を進めているアンチmiRNA核酸は、これまでに開発されてきた筋ジストロフィー治療用核酸医薬とは作用機序が異なっており、患者さんの遺伝子変異のタイプによらず効果が期待されます。
これまでの研究から、それぞれのシーズにおいて有効性と安全性を兼ね備えた有望な候補配列が見出されてきており、今後の最適化のステップを経て、R7年度中に最終候補配列を選定します。その後、製造法検討や分析法検討等のCMC検討を進め、非臨床試験を実施しこれら2つの核酸医薬シーズの「臨床ステージアップ」を目指します(図3)。
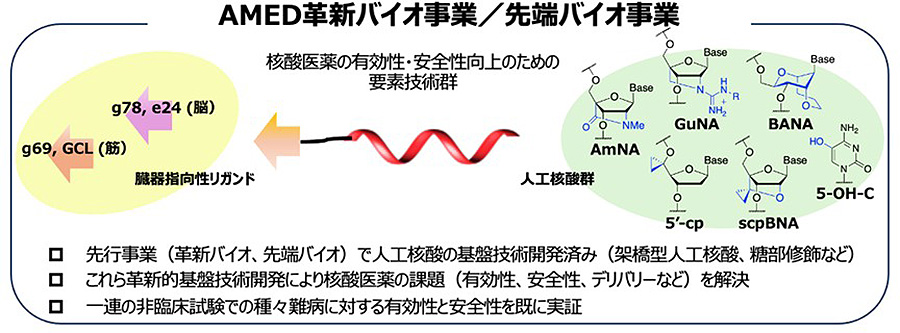
図1. 先行事業(AMED革新バイオ事業/先端バイオ事業等)での研究成果
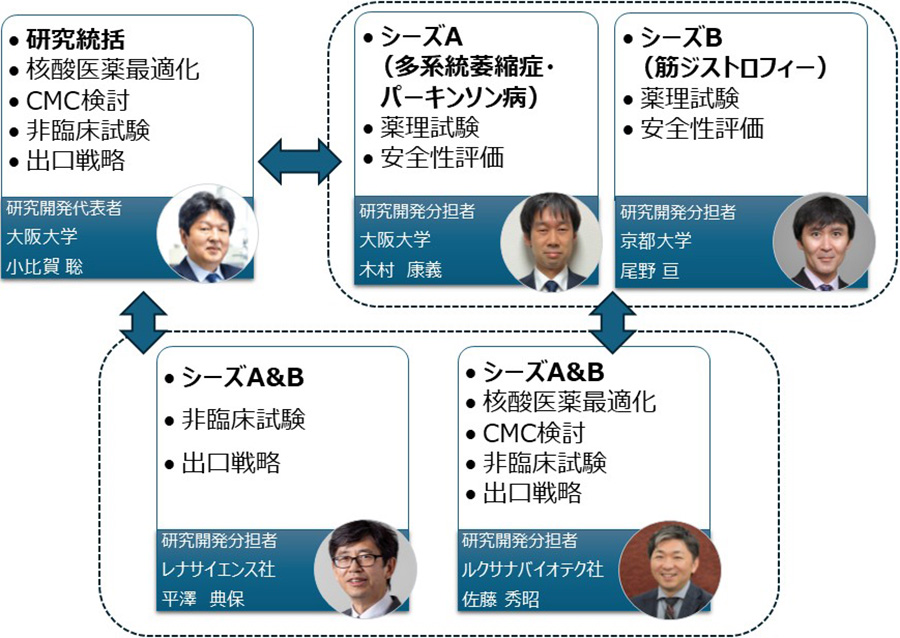
図2. 本研究開発課題の実施体制
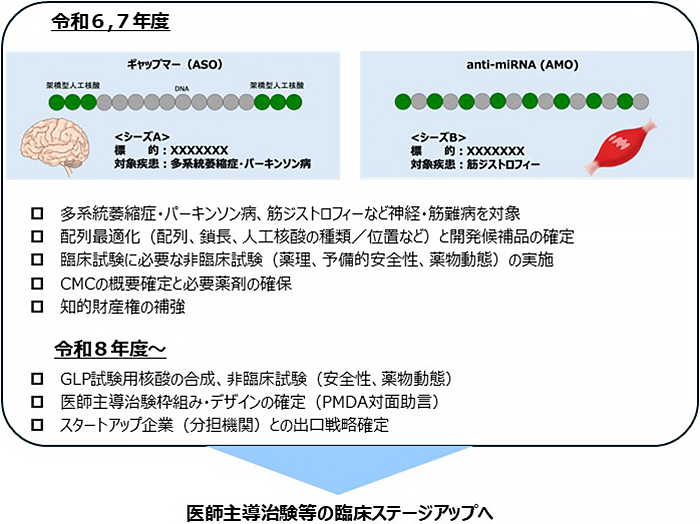
図3. 本研究開発課題の計画概要